
編譯 | 陳駿達
編輯 | Panken
智東西2月20日報道,用48小時破解生物學家苦心鑽研10年的「超級細菌」難題,還可免費申請使用,這是谷歌研究院(Google Research)昨日在AI for Science領域發布的最新成果:一個基於Gemini 2.0構建的AI協作科學家。
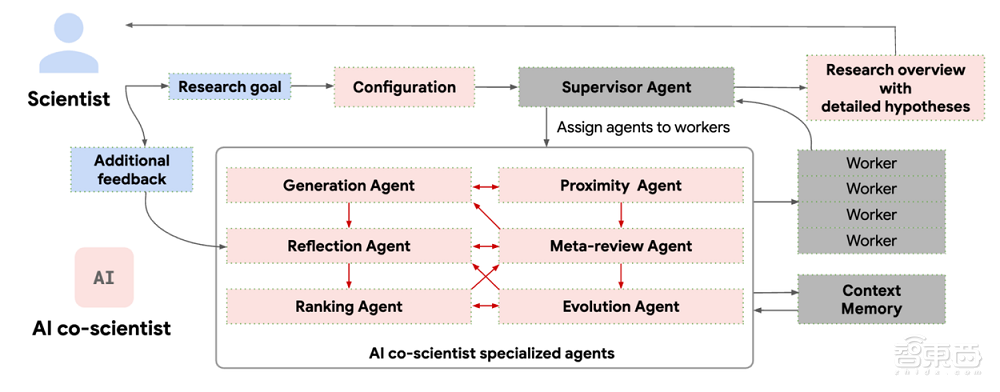
▲AI協作科學家架構(圖源:谷歌)
谷歌此番發布的AI協作科學家基於多智能體系統,能作為虛擬科研合作者,幫助科學家生成新穎的假設和研究提案。
在實際測試中,AI協作科學家已經展現出驚人的實力:它獨立提出了一個關於細菌基因轉移機制(耐藥性)的新穎假設,發現了一款白血病治療再利用候選藥物,還識別出了肝纖維化治療的遺傳學靶點。
這些研究之前從來沒有發表過,這表明AI協作科學家是自主得出這一見解的。
谷歌AI協作科學家完成的上述科研任務被專業人員界定為中等到超高難度。參與驗證的科學家稱,AI雖然無法進行證明假設的實驗,但如果能在項目開始之初就得到相關假設,那麼就能節省幾年的工作。
AI協作科學家能生成並驗證研究假設,通過模擬辯論和完善假設,構建知識網絡並進化假設,最終生成研究概述供科學家審查。這一系統的目的不是完全取代人類科學家,人類能夠全程參與並指導AI的推理過程,從而更好地滿足科研實際需求。
目前,谷歌已經將AI協作科學家測試版免費提供給研究人員,並且還將發布一個API接口,以允許網站使用其基礎技術。

▲AI協作科學家論文(圖源:谷歌)
論文地址:
https://storage.googleapis.com/coscientist_paper/ai_coscientist.pdf
一、跨學科合作推動科學發現,AI協作科學家適用於多個領域
科學發現的過程一直依賴於跨學科的合作,這種模式在歷史上促成了許多重大的科學突破。
谷歌研究院團隊認為,隨着大語言模型的發展、AI多模態理解能力的提升,科學家們現在可以使用這些技術,幫助他們跨越學科的界限,整合不同領域的知識和數據。
此前,獲得諾貝爾獎的谷歌DeepMind CEO Demis Hassabis和研究總監John Jumper等人,通過發明AlphaFold徹底改變了生物學研究的遊戲規則,這一系統能預測蛋白質結構,大幅度節省研究時間。此外,也有不少研究者開發了類似的AI工具。
不過,現有的AI系統在科學發現中的應用仍存在侷限性。例如,一些系統依賴於回顧性數據,缺乏端到端驗證;另一些系統雖然在文獻總結方面表現出色,但在生成新的科學假設方面能力不足。
谷歌研究院此番推出的AI協作科學家通用性更強,適用於多個研究領域,不僅能夠進行文獻探索和假設驗證,還能通過模擬科學辯論和自我批判來完善假設,從而加速科學發現的進程。這一系統還能結合專家反饋和實驗室驗證,確保生成的假設不僅新穎,而且具有實驗驗證的可行性。
他們的目標不是將科學發現工作完全自動化,而是為科學家打造一個強大的AI協作者。這一系統通過靈活的自然語言交互和專家反饋機制,確保科學家能夠全程參與並指導AI的推理過程,從而更好地滿足科學家的實際需求。
二、多智能體協作進行科研,不斷自我批評、迭代
AI協作科學家系統由多個智能體組成,每個智能體負責不同的任務,包括生成假設、反思假設、排名假設、進化假設等。系統的核心是通過生成、辯論和進化的方法,結合科學方法的啓發,利用計算資源的擴展來加速假設生成。
系統的設計包括以下幾個關鍵組件:
1、自然語言交互界面(Natural Language Interface)
科學家通過自然語言與系統交互,定義研究目標、提供反饋、提出自己的想法,並指導系統的推理過程。
2、異步任務執行框架(Asynchronous Task Execution Framework)
系統採用異步任務隊列管理多個智能體的工作流程。監督智能體(Supervisor Agent)負責分配任務、管理資源,並根據需要動態調整計算資源的分配。
3、專用智能體(Specialized Agents)
系統由多個智能體組成,每個智能體負責特定的推理任務,共同協作生成高質量的研究假設和實驗方案。這些智能體包括:
生成智能體(Generation Agent):負責生成初始假設和研究提案。
反思智能體(Reflection Agent):對生成的假設進行評估和審查,確保其合理性、新穎性和可行性。
排名智能體(Ranking Agent):通過錦標賽機制對假設進行排名,比較不同假設的優劣。
進化智能體(Evolution Agent):通過改進和優化排名靠前的假設,提升其質量。
相似性智能體(Proximity Agent):計算假設之間的相似性,幫助組織錦標賽並探索假設空間。
元評審智能體(Meta-review Agent):總結錦標賽中的反饋和模式,優化其他智能體的表現,並生成研究概述。
4、上下文記憶(Context Memory)
系統使用持久化上下文記憶來存儲和檢索智能體和系統的狀態,支持長周期的迭代計算和科學推理。
5、工具使用(Tool Use)
系統能夠調用外部工具(如網絡搜索、專用AI模型等),以增強生成假設的依據和質量,確保其科學性和可行性。
6、科學家反饋(Scientist Feedback)
科學家可以通過自然語言提供反饋,直接參與系統的推理過程,指導系統生成更符合需求的假設和研究方案。
7、研究概述生成(Research Overview Generation)
元評審智能體將排名靠前的假設總結為詳細的研究概述,供科學家進一步評估和指導後續研究。

這一系統的高質量回答得益於其推理過程中使用的大量計算資源,也就是所謂的測試時計算(Test-time Compute)。測試時計算主要用於迭代推理、演化和改進輸出。
關鍵推理步驟包括基於自博弈的科學辯論以生成新假設、排名錦標賽以比較假設,以及一個用於質量改進的「進化」過程。系統的Agent性質促進了遞歸自我批評,包括使用工具進行反饋以細化假設和提案。
系統的自我提升依賴於從錦標賽中得出的Elo自動評估指標。谷歌團隊在GPQA diamond基準測試上驗證了,更高的 Elo評級與正確率呈正相關。
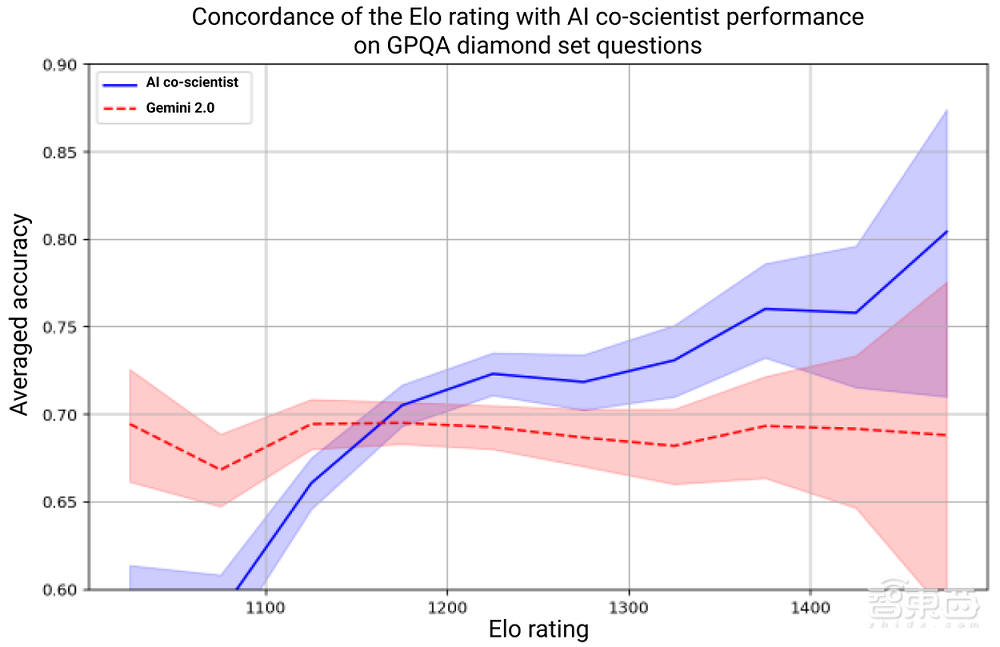
在科研問題上,谷歌讓7位人類專家策劃15個開放性研究目標,並讓人類專家給出最佳的假設解決方案。通過自動化的Elo評估指標,AI協作科學家在解決這些複雜問題時超越了其他最先進的智能體和推理模型。
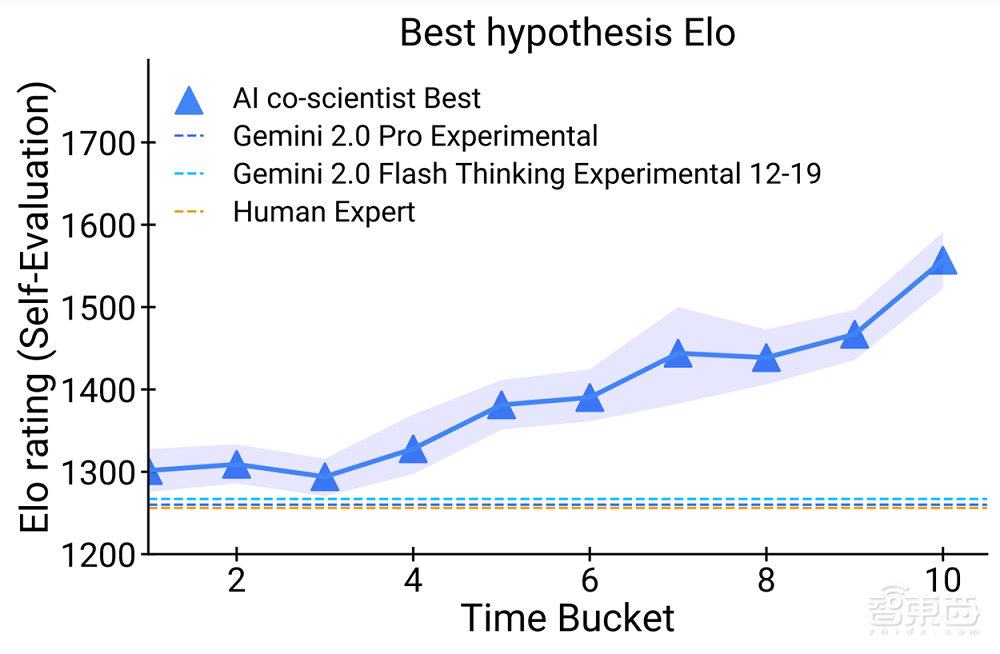
擴展測試時計算在這一測試中得到了鮮明的展現。隨着系統投入更多時間進行推理和改進,其自動評估結果質量逐漸提升,最終超越了其他模型和未經輔助的人類專家。
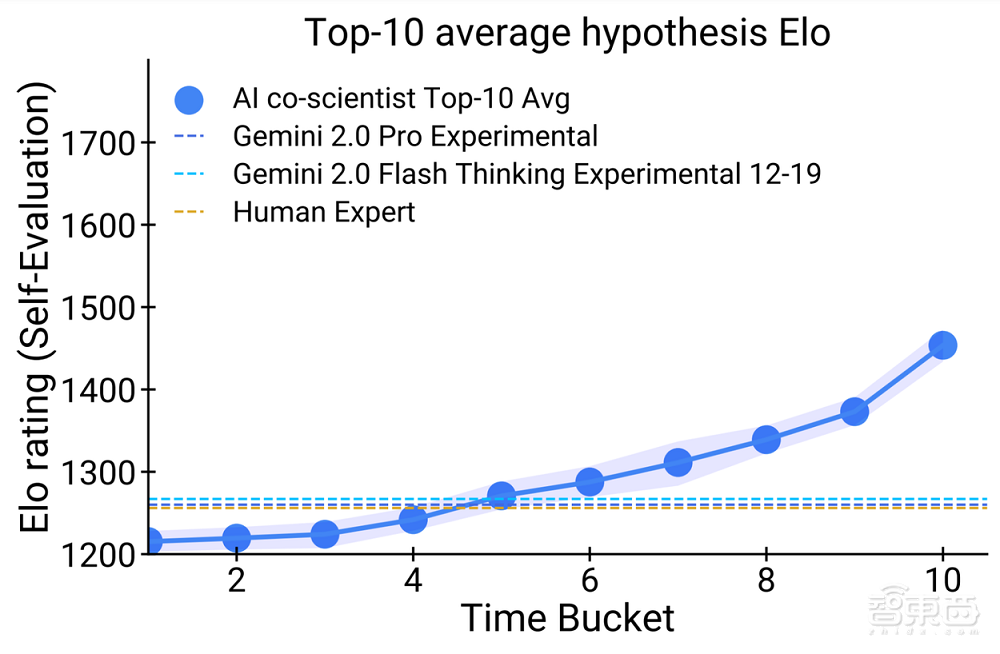
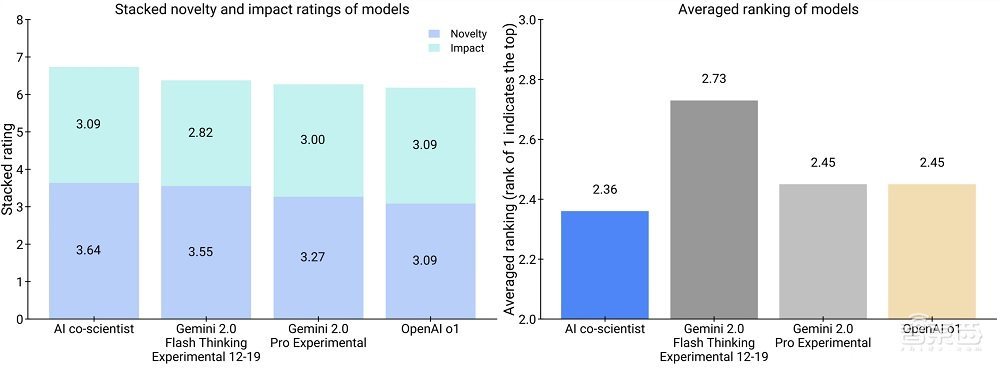
在11個研究目標上,專家們對AI協作科學家生成的結果與其他相關基線模型進行了比較,評估了其新穎性和影響力,並給出了總體偏好的評價。
儘管樣本量較小,但專家們認為AI協作科學家在新穎性和影響力方面具有更高的潛力,並且更傾向於信任其輸出結果。此外,這些人類專家的偏好與之前的Elo自動評估指標相一致。
三、可解決超高難度科研問題,回溯數十年文獻得出新假設
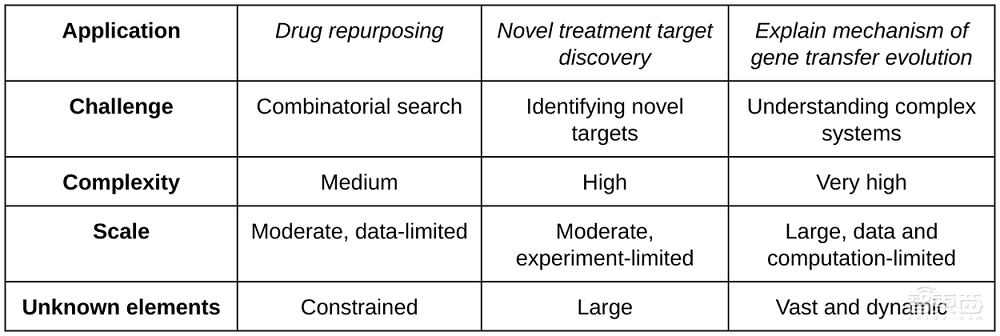
谷歌在三個關鍵生物醫學領域對AI協作科學家生成的假設和研究方案進行了端到端的實驗室驗證:藥物再利用(中等難度)、提出新的治療靶點(高難度),以及闡釋抗菌素耐藥性的機制(超高難度)。這些驗證過程均在專家指導下進行。
1、急性髓系白血病的藥物再利用
藥物開發是一個日益耗時且成本高昂的過程,針對每種疾病或適應症,都需要重新啓動發現和開發過程的許多環節。藥物再利用通過發現現有藥物的新治療用途來應對這一挑戰,但這一任務的複雜性要求具備廣泛的跨學科專業知識。
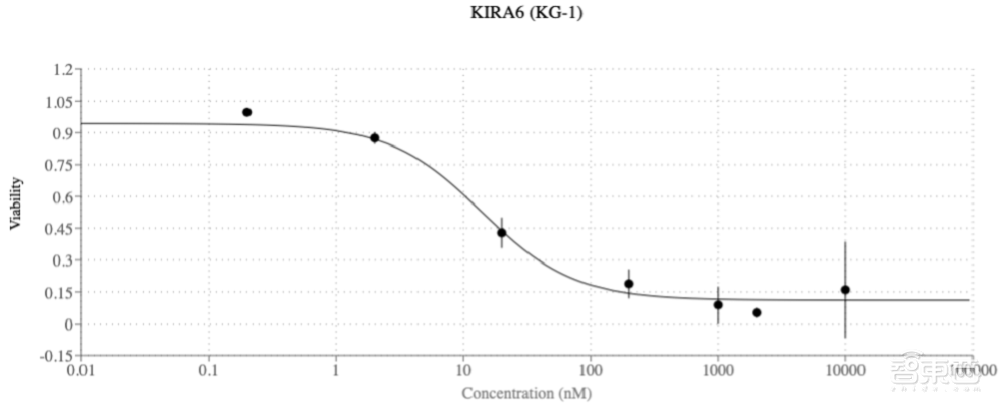
谷歌的AI成功為急性髓系白血病(AML)提出了新的再利用候選藥物,後續實驗驗證了這些提議,確認所建議的藥物在多種AML細胞系中以臨牀相關濃度(能達到預期效果的最低或最高濃度)抑制腫瘤活性。
相關論文:
https://storage.googleapis.com/coscientist_paper/penades2025ai.pdf
2、肝纖維化的靶點發現
與藥物再利用相比,發現新的治療靶點更為複雜,面臨低效的假設選擇過程和實驗驗證的優先級排序不佳等問題。AI輔助靶點發現有助於簡化實驗驗證的過程,最終減少開發時間和成本。
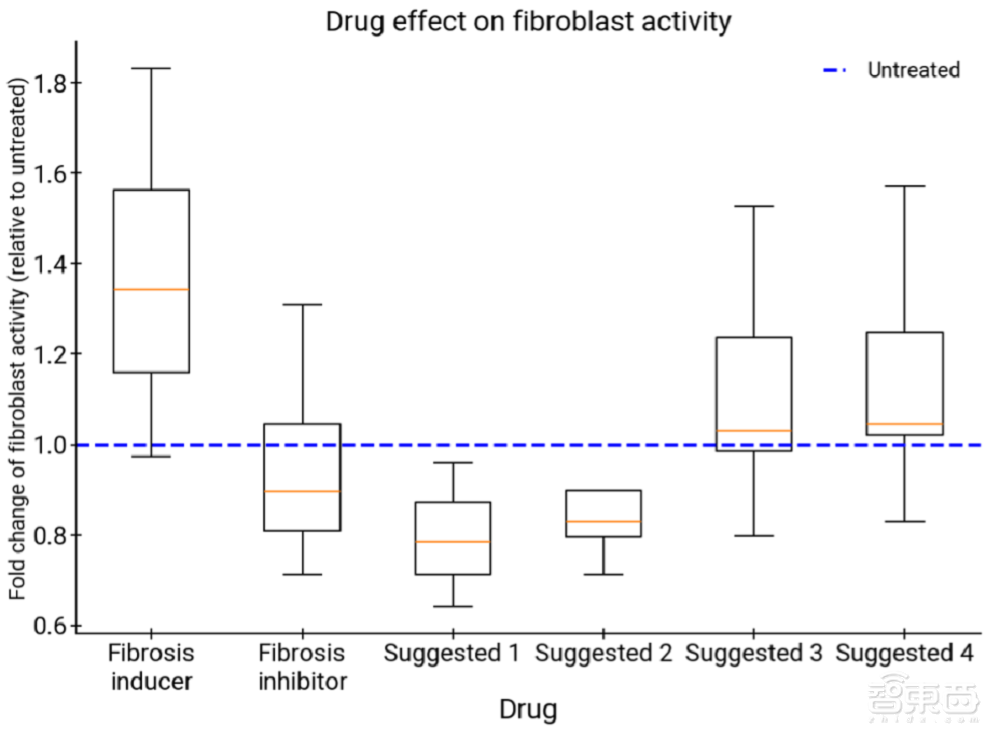
AI協作科學家通過識別基於臨牀前證據的表觀遺傳學靶點,展示了其潛力,這些靶點在人類肝臟類器官(由人類細胞衍生的3D多細胞組織培養,旨在模擬人類肝臟的結構和功能)中顯示出顯著的抗纖維化活性。這些發現將在斯坦福大學合作者主導的即將發布的報告中詳細介紹。
3、抗菌素耐藥性的機制闡釋
第三個驗證案例聚焦於生成假設以解釋與抗菌素耐藥性(AMR)相關的細菌基因轉移進化機制——即微生物進化出的抵抗感染治療藥物的機制。
這是一個複雜的挑戰,需要理解基因轉移的分子機制(接合、轉導和轉化)以及推動 AMR 基因傳播的生態和進化壓力。
在這一測試中,專家研究人員指導AI協作科學家探索其團隊已經發現,但尚未公開的研究主題,即解釋為什麼噬菌體誘導的染色體島(cf-PICIs)存在於多種細菌物種中。
AI協作科學家系統獨立提出,cf-PICIs通過與多種噬菌體尾部的相互作用,來擴大其宿主範圍。這一發現已經在研究人員之前的原始實驗中得到了驗證。
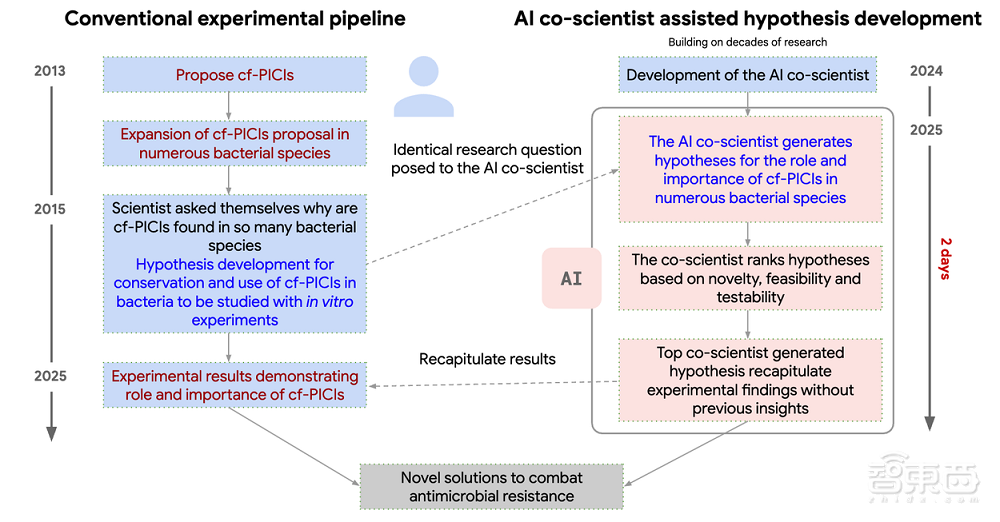
這一計算機模擬發現已在使用AI協作科學家系統之前進行的原始實驗室實驗中得到實驗驗證。
這展示了AI協作科學家系統作為輔助技術的價值,它能夠利用同一研究主題上的所有開放權限的文獻,在數十年研究成果的基礎上做出新的判斷。
結語:AI進一步加速科學發現
谷歌研究團隊提出,未來他們還將進一步增強AI協作科學家在文獻綜述、事實覈查、連貫性檢查方面的能力,也會讓更多領域的專家參與到系統的改進過程中,提升其可用性與可信度。
此外,強化學習、多模態數據整合、實驗室自動化集成等方向的探索,將讓現有系統的能力進一步提升,能更加端到端地完成複雜科研任務,進一步加速科學發現。