智通財經APP獲悉,2月25日,中國國家藥監局藥品審評中心(CDE)官網最新公示,賽諾菲(SNY.US)申報的鹽酸非索非那定口服混懸液新適應症上市申請獲得受理。此前非索非那定片已經在中國獲批,用於治療過敏性鼻炎及慢性特發性蕁麻疹。
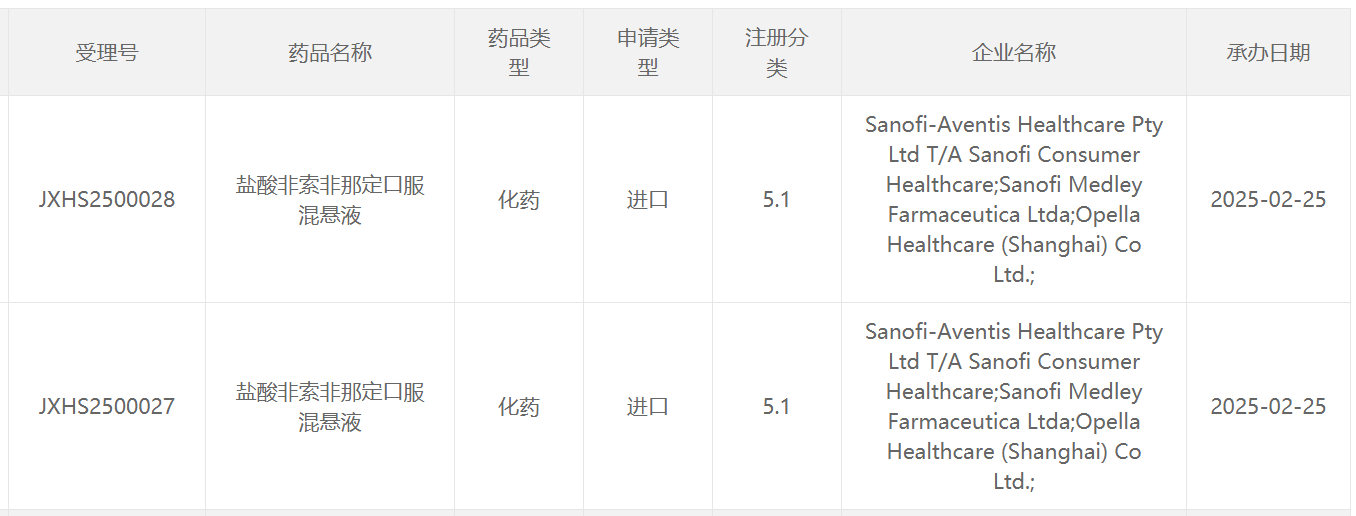
本次申報上市的為口服混懸液劑型,同時這也是口服混懸液劑型在中國的第二項上市申請。根據賽諾菲此前新聞稿,美國FDA此前已批准鹽酸非索非那定口服混懸液用於治療2~11歲兒童季節性過敏相關症狀,以及6個月~11歲兒童慢性特發性蕁麻疹。由此推測,口服混懸液劑型在中國兩次申報的適應症也可能為兒童季節性過敏及慢性特發性蕁麻疹。相比於片劑劑型,口服混懸液因其口感好、易於吞嚥,有可能為兒童患者提供更方便的治療選擇。
根據賽諾菲公開資料介紹,非索非那定是二代新型抗組胺藥,兼具拮抗組胺和抗炎作用,具有起效快、24小時長效,且不引起嗜睡,腦部受體佔有率低等特點。其對H1受體的親和力較高,表明其較好的心臟安全性。
從作用機制來看,組胺H1受體主要分佈於血管內皮、氣道平滑肌等多種細胞,與過敏反應的關係非常密切。靶向組胺H1受體的抗組胺藥可將被組胺激活的受體下調至未激活的狀態,下調過敏性炎症,減少促炎症細胞因子和細胞黏附分子的表達,並減弱嗜酸性粒細胞等的趨化作用,進而發揮生物學效應。