炒股就看金麒麟分析師研報,權威,專業,及時,全面,助您挖掘潛力主題機會!

《電鰻財經》文 / 李瑞峯
2024年12月31日,上海恒潤達生生物科技股份有限公司(以下簡稱恒潤達生)科創板更新了招股說明書。招股書顯示,恒潤達生是專注於突破性免疫細胞治療產品研發與生產的創新生物醫藥公司,其主營產品為CAR-T 細胞治療產品,產品主要聚焦惡性血液病和實體腫瘤等治療領域。
在研究該公司提供的上市資料時,《電鰻財經》注意到,此次IPO,恒潤達生擬將6億元募集資金用於補充流動資金,而截至2024年6月30日的財務數據顯示,該公司的資產總額僅為3.4億元,這一數字幾乎只相當於其募集計劃的一半。目前,恒潤達生尚處於無收入、無利潤的境地,每年卻需傾注鉅額現金於研發之中,靜候其研發投入結出碩果。然而,令人遺憾的是,自2018年以來近六年的時間跨度內,該公司僅取得了三項發明專利,這一成果顯然不盡如人意。此外,從產業視角審視,國內CAR-T的商業化之路依舊佈滿荊棘,面臨着多重嚴峻挑戰。
6億募資補流 為總資產兩倍 7高管薪酬合超千萬
招股書清晰披露,恒潤生達在本次IPO中計劃募集高達25.4億元資金,其中,13.4億元將專項投入腫瘤免疫細胞治療產品的研發項目,另有6億元將用於總部及產業化基地的建設,而剩餘的6億元則旨在補充公司的流動資金,佔總募集資金的四分之一。
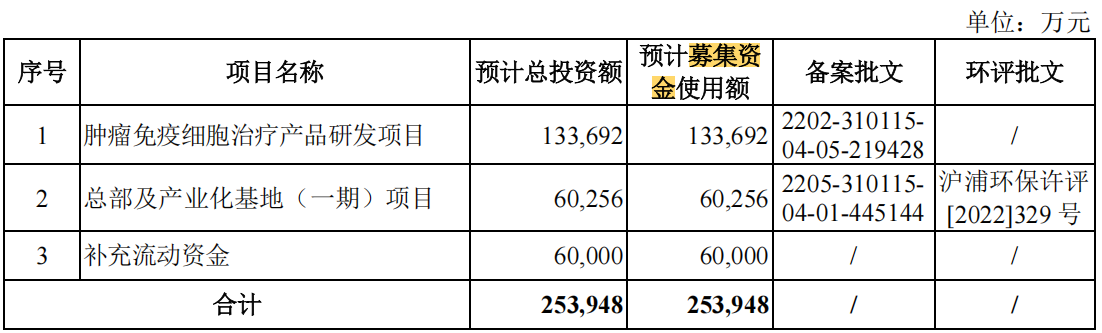
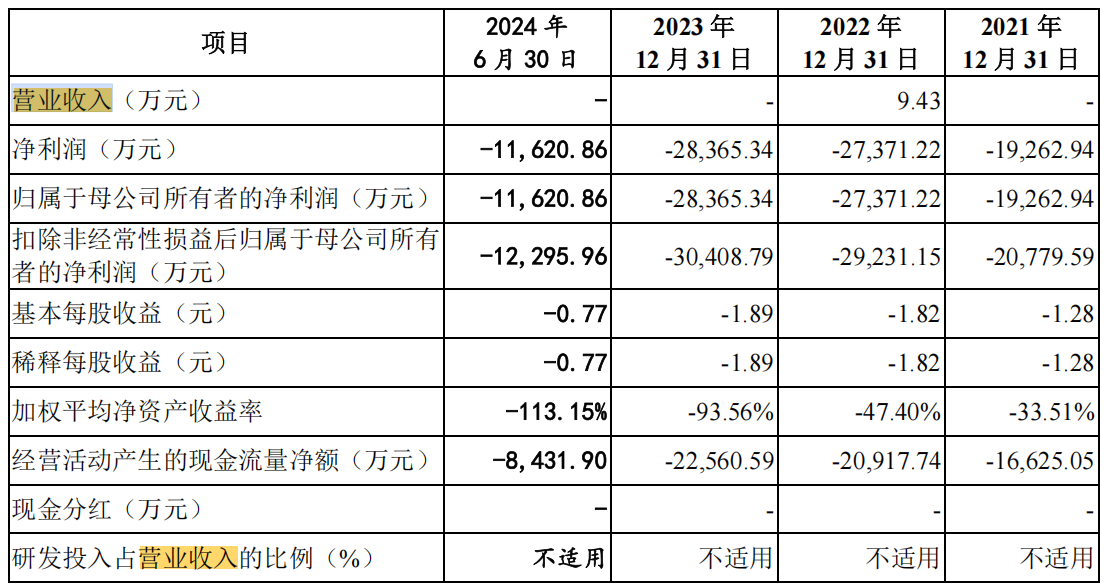
截至目前,恒潤生達尚未實現產品的商業化。在2021年至2023年及2024年上半年的報告期間內,公司僅在2022年取得了微薄的營業收入9.43萬元。同時,公司的經營活動現金流量淨額在此期間分別為-1.66億元、-2.09億元、-2.26億元和-0.84億元,顯示出公司在報告期內幾乎沒有收入,且需持續投入大量現金以維持運營。
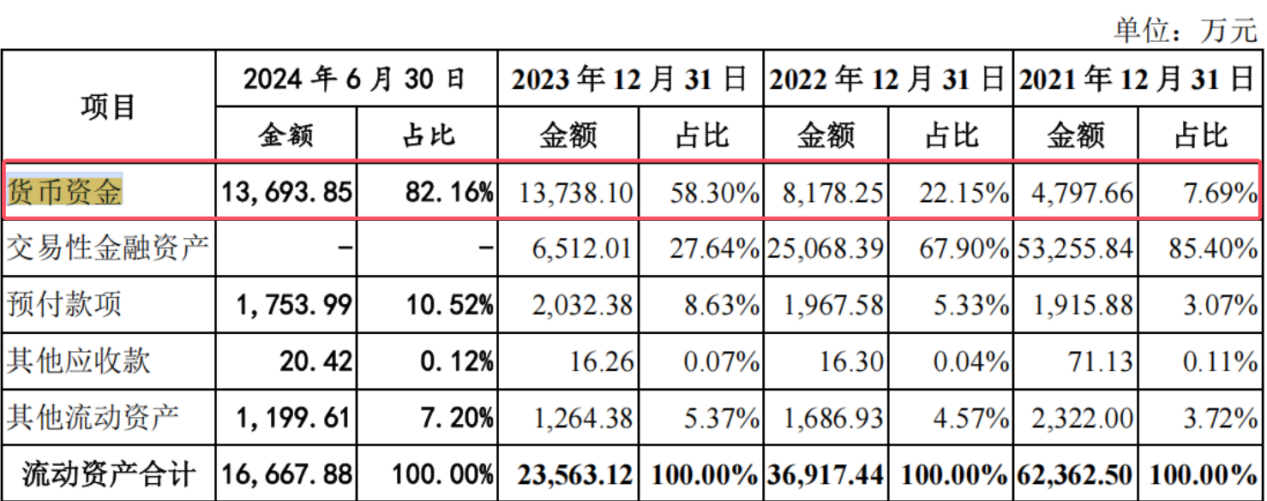
值得注意的是,恒潤生達的貨幣資金量在報告期內呈現顯著增長趨勢。各期末,該公司的貨幣資金量分別為4797.66萬元、8178.25萬元、13738.1萬元和13693.85萬元,佔當期流動資產的比例也逐期攀升至7.69%、22.15%、58.3%和82.16%。這一增長主要得益於公司在2021年4月的增資行為,當時公司新增14名股東,共計收到增資6.73億元,其中實收資本1.55億元,新增資本公積金6575萬元,為公司的運營提供了有力補充,但仍難以滿足其龐大的資金需求。
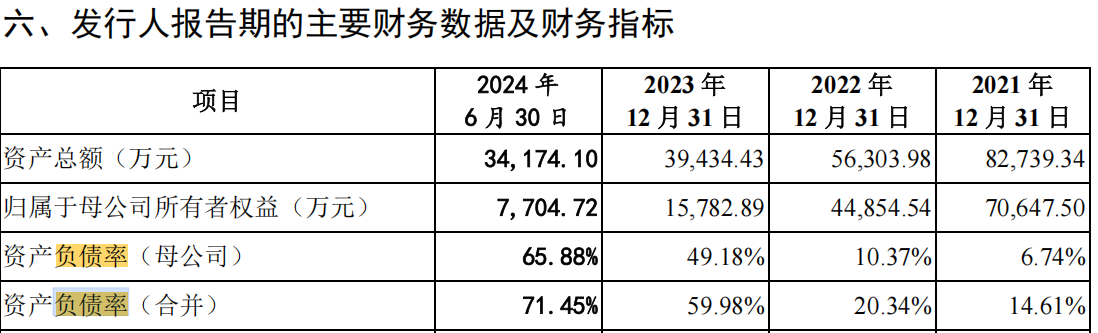
此外,恒潤生達還享受着政府的鉅額補助。報告期內,該公司分別獲得政府補助879.8萬元、645.87萬元、1622.33萬元和418.47萬元。然而,儘管有這些補助,該公司的資產負債率仍在持續飆升,報告期內分別高達6.74%、10.37%、49.18%和65.88%。
在公司經營需要持續投入且業績持續虧損的背景下,恒潤生達的高管薪酬卻頗為可觀。報告期內,該公司董事、監事、高級管理人員及核心技術人員的薪酬合計分別為1129.92萬元、1481.45萬元、1309.67萬元和544.68萬元,而當期利潤總額卻分別為-1.93億元、-2.74億元、-2.84億元和-1.19億元。
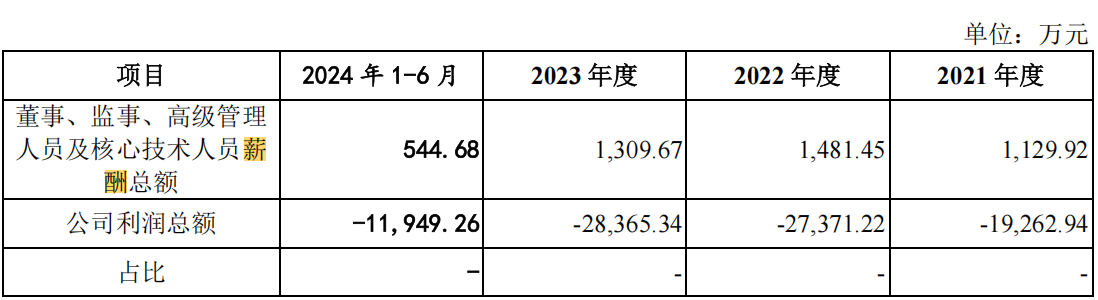
特別值得一提的是,該公司有7位高管的薪酬超過百萬。2023年,副董事長、副總經理李國清年薪134.27萬元,董事、總經理黃飛年薪高達215.27萬元,副總經理李國棟年薪164.81萬元,董事會祕書仇英德年薪134.47萬元,財務負責人朱照錦年薪104.47萬元,首席醫學官王丹紅年薪121.28萬元,研發高級總監年薪更是達到128.92萬元。這七位高管的薪酬合計超過千萬元,引人關注。
六年僅獲三項發明專利
在沒有收入、利潤及經營現金流的艱難處境下,恒潤生達依然矢志不渝地加大研發力度,以期迅速推進產品的商業化進程。在報告所覆蓋的期間內,該公司的研發費用節節攀升,分別達到了1.6億元、2.4億元、2.6億元和8988萬元。
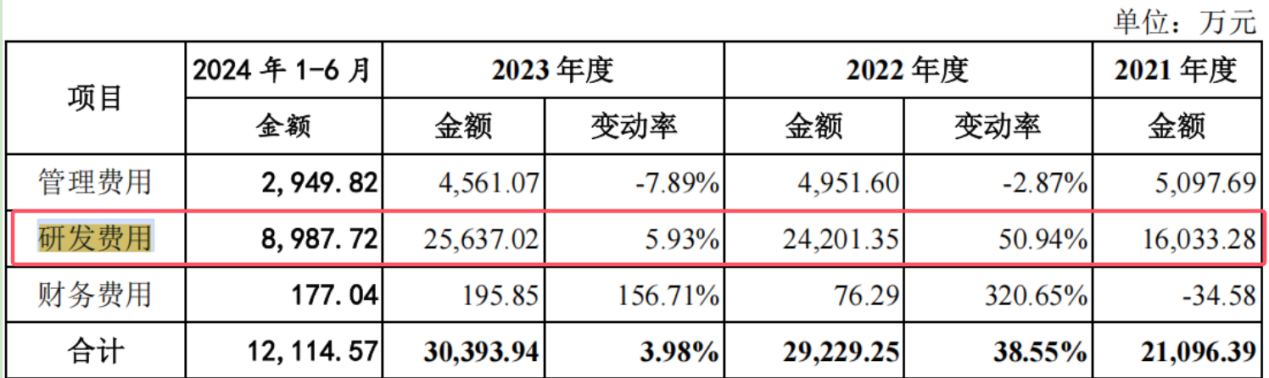
然而,儘管恒潤生達在研發上的投入持續增長,但其研發成果卻顯得略為遜色。招股書清晰顯示,截至報告期末,恒潤生達及其子公司共獲得了63項境內專利授權,這其中包括了39項發明專利與24項實用新型專利,然而,境外專利的授權卻仍為空白。
尤為值得注意的是,在恒潤生達所擁有的39項發明專利中,絕大多數均為2019年之前所取得。自2019年起,該公司的發明專利新增數量顯著放緩,僅在2020年7月、2021年10月和2022年6月分別獲得了三項發明專利。
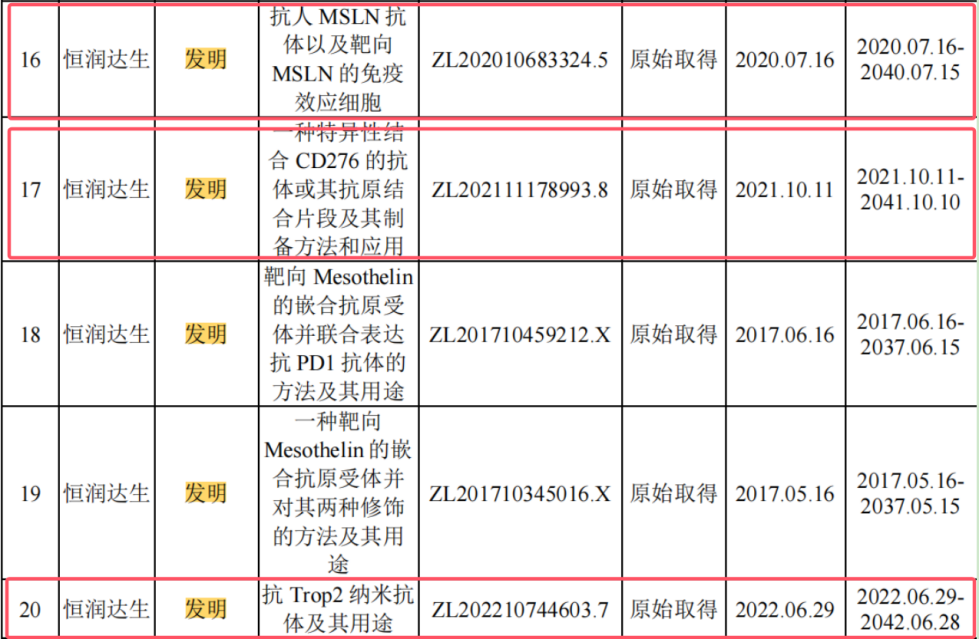
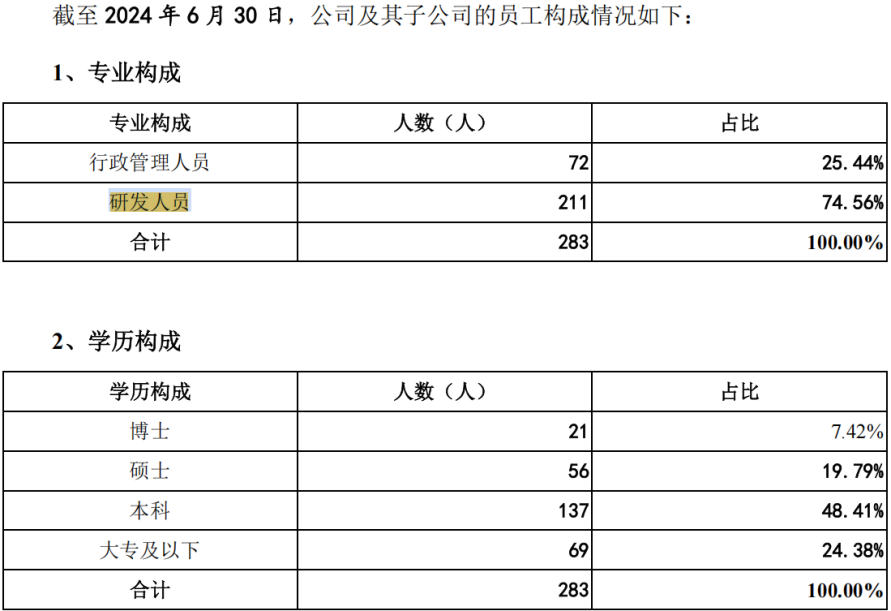
由此可見,從2019年至2024年,該公司在約六年時間內僅獲得三項發明專利。在研發成果並不十分亮眼的情況下,恒潤生達的研發團隊卻佔據了公司員工的絕大多數。截至2024年6月30日,該公司的研發人員數量已達72人,佔員工總數的比例高達74.56%。
國內CAR-T行業仍面臨多重挑戰
恒潤生達全部「押寶」CAR-T行業,但目前A股資本市場上,尚未有單獨依靠CAR-T技術而實現上市的企業。究其原因,尚不明朗的商業化前景是阻礙相關公司上市的重要因素。
目前我國CAR-T行業核心技術依賴進口,產業鏈自主可控性不足。首先,CAR-T生產所需的關鍵設備(如細胞培養設備)和核心原材料(如病毒載體、質粒)仍主要依賴進口,國產替代率較低。例如,慢病毒載體技術長期被海外企業壟斷,導致生產成本居高不下且供應鏈穩定性不足。而且,病毒載體和細胞培養試劑佔生產成本的30%-50%,國內企業議價能力弱,易受國際供應鏈波動影響。
其次,國內CAR-T療法多集中於CD19、BCMA等成熟靶點,同質化競爭嚴重。例如,2023年國內臨牀試驗中涉及CD19的佔比超過70%,而實體瘤靶點研發進展緩慢。通用型CAR-T(異體療法)和實體瘤治療技術仍處於早期階段,難以突破免疫排斥和腫瘤微環境複雜性的難題。
目前高成本與支付難題也制約着CAR-T的商業化。首先,國內已上市的CAR-T產品定價在120萬-129萬元/針,遠超普通患者支付能力。例如,藥明巨諾的倍諾達2023年銷售毛利率雖提升,但年銷售額僅8774萬元,反映出市場滲透率低。而且,醫保覆蓋有限,目前僅有部分城市惠民險和商業保險嘗試覆蓋,但賠付比例和覆蓋人羣有限,患者自費壓力大。
此外,CAR-T需「一對一」定製化生產,無法批量製造,人工操作佔比高。單批次生產需耗時2-3周,且對實驗室人員技術要求嚴格,導致單位成本難以降低。
CAR-T行業的AR-T臨牀需求與市場拓展受限。國內獲批的CAR-T產品均針對血液系統腫瘤(如淋巴瘤、多發性骨髓瘤),而佔癌症患者90%的實體瘤領域尚未突破,技術瓶頸包括靶點特異性不足、腫瘤微環境抑制T細胞活性等。目前僅少數三甲醫院具備CAR-T治療資格,且需通過嚴格的資格認證和冷鏈運輸管理。截至2024年,全國具備資格的醫院不足200家,限制了療法的可及性。
CAR-T行業競爭加劇並存在監管風險。目前國內CAR-T研發企業已近百家,但多數聚焦於相同靶點和適應症。例如,CD19靶點的同質化競爭已呈現類似PD-1的激烈態勢,未來可能出現價格戰和資源浪費810。2023年FDA調查發現CAR-T療法可能誘發T細胞惡性腫瘤風險(如淋巴瘤),儘管尚無直接證據,但已引發市場對長期安全性的擔憂。國內監管部門或跟進加強安全性審查,延長臨牀試驗觀察期,增加企業研發成本。此外,副作用管理(如細胞因子釋放綜合徵CRS、神經毒性ICANS)仍是技術難點,需投入更多資源優化治療方案。
CAR-T行業還面臨國際化競爭和出海挑戰。目前國產CAR-T產品需滿足國際監管標準(如FDA、EMA),但國內臨牀試驗數據積累不足,技術驗證難度大。例如,傳奇生物的Carvykti雖在美國獲批,但需依賴強生的全球渠道資源。海外市場支付體系(如商業保險覆蓋)雖更完善,但競爭激烈,國內企業需面對諾華、吉利德等巨頭的直接挑戰。
從競品的銷售數據看,以同為國產的藥明巨諾的倍諾達為例,該產品於2021年9月獲批上市,2021年-2023年全球銷售額分別為0.31億元、1.46億元、1.74億元,2023年產品營收增速已顯著放緩。由此可見,產品上市只是起點,商業化驗證仍然是恒潤達生必須面對的終極考驗。
《電鰻快報》