智通財經APP獲悉,4月3日,中國國家藥監局藥品審評中心(CDE)官網最新公示,阿斯利康(AZN.US)申報的本瑞利珠單抗注射液一項新適應症上市申請獲得受理,具體適應症尚未披露。公開資料顯示,本瑞利珠單抗(benralizumab)是阿斯利康開發的一款靶向IL-5受體的單克隆抗體,此前已經在中國獲批用於成人和12歲及以上青少年重度嗜酸粒細胞性哮喘的維持治療。在美國,該產品還已經獲FDA批准用於治療嗜酸性肉芽腫性多血管炎(EGPA)的成年患者。
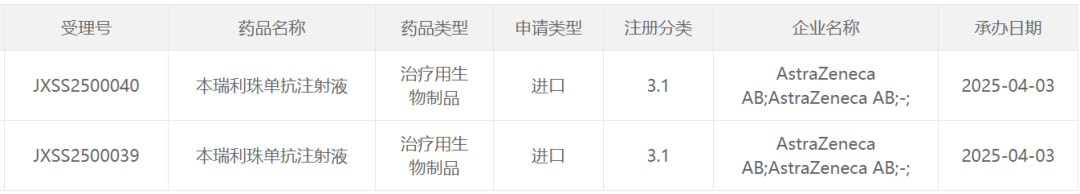
截圖來源:CDE官網
根據阿斯利康近期新聞稿介紹,本瑞利珠單抗重度嗜酸粒細胞性哮喘(SEA)適應症目前已在美國、歐盟、日本、中國等80多個國家和地區獲批。嗜酸性肉芽腫病伴多血管炎(EGPA)適應症也已經在美國、歐盟和日本等全球35多個國家和地區獲批。阿斯利康也在對該產品的其它適應症進行開發,包括慢性阻塞性肺疾病(COPD)和嗜酸粒細胞增多綜合徵。本次本瑞利珠單抗新適應症在中國申報上市,意味着其有望在不久的將來惠及更多患者。