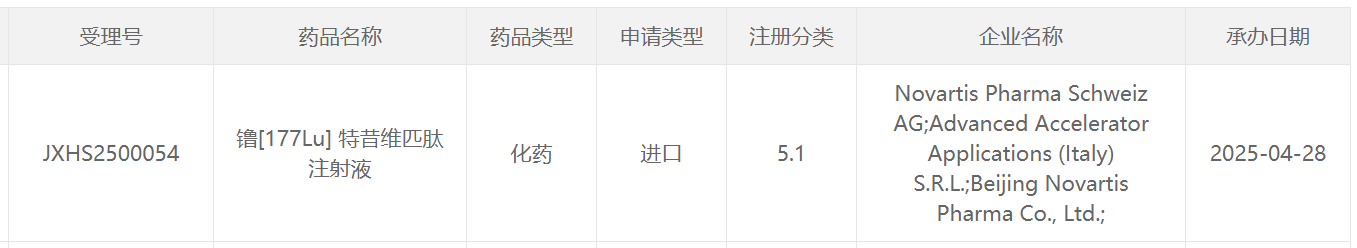
智通財經APP獲悉,4月28日,中國國家藥監局藥品審評中心(CDE)官網最新公示,諾華(NVS.US)申報的鑥[177Lu] 特昔維匹肽注射液一項新適應症上市申請獲得受理。公開資料顯示,這是諾華研發的靶向PSMA的放射配體療法(RLT)Pluvicto(lutetium Lu 177 vipivotide tetraxetan) 。該藥此前已經在中國申報首個適應症上市申請,並被CDE納入優先審評,用於治療PSMA陽性轉移性去勢抵抗性前列腺癌(mCRPC) 、已接受雄激素受體通路抑制和紫杉類化療的成年患者。
根據諾華公開資料可以推測,本次該藥申報上市的適應症為:用於更早線未經化療的PSMA陽性的mCRPC患者。針對該項適應症,Pluvicto於今年4月獲得了美國FDA批准。
Pluvicto是通過靜脈注射的放射配體療法(RLT),由靶向配體與治療性放射性核素(鑥-177)結合而成。進入血液後,Pluvicto可靶向結合表達PSMA的前列腺癌細胞。結合後,放射性同位素釋放的能量可破壞靶細胞,抑制其複製能力和/或引發腫瘤細胞死亡。