2月27日,映恩生物再度递表港交所,Morgan Stanley、Jefferies、CITIC Securities为其联席保荐人。此前,映恩生物曾于2024年8月26日递表港交所,于2月26日失效。
值得关注的是,今年开年,映恩生物就迎来利好,再一次实现ADC出海。1月8日,映恩生物以5000万美元首付款,最高11.5亿美元里程碑款的价格,将EGFR/HER3双抗ADC DB-1418授权给Avenzo Therapeutics。
此次映恩生物能否再添喜事,获得港股“通行证”呢?
手握12款ADC药物ADC出海提速
招股书显示,映恩生物成立于2019年,是抗体偶联药物(“ADC”)领域的全球领跑者,致力于为癌症和自身免疫性疾病等患者研发新一代ADC创新药物。公司利用自身的ADC技术平台,已建立起各种具有差异化的管线,公司正在推进这些管线,目标是革新癌症治疗模式,并提供可显著改善全球患者治疗效果的疗法。
目前,公司拥有自主研发的两款核心产品,即DB-1303/BNT323(一款靶向HER2癌症(包括子宫内膜癌及乳腺癌)的HER2 ADC候选药物)及DB-1311/BNT324(一款靶向B7-H3癌症(包括小细胞肺癌、去势抵抗性前列腺癌及食管鳞状细胞癌)的B7-H3 ADC候选药物)。
除核心产品外,公司还自主研发了:五款其他临床阶段ADC,在广泛适应症中具有潜力,根据Frost & Sullivan,就总体或主要适应症的开发进展而言,每款均跻身全球临床最领先之列;两款新一代双特异性ADC预计将于2025年至2026年进入临床阶段;及多款其他临床前ADC。

截至2月19日,公司有五项处于临床阶段的资产已获得美国食品药品管理局(“FDA”)及中国国家药品监督管理局(“中国药监局”)的研究用新药批准。公司在17个国家的230多个临床试验中心拥有七项全球多区域临床试验,已有2000多名患者(超过50%位于美国、欧盟及澳大利亚)入组。公司的创新ADC资产已吸引全球领先的生物制药公司,迄今为止已建立数个全球合作伙伴关系,包括与BioNTech SE、百济神州有限公司、Adcendo ApS 、GSK plc及Avenzo Therapeutics, Inc.的合作,交易总价值逾60亿美元(其中截至最后实际可行日期已收到约400百万美元)。
尽管手握12款ADC药物,但映恩生物没有商业化产品上市,收入主要就是靠对外授权。映恩生物披露,目前就其ADC相关资产建立的合作,交易里程碑总价值已超40亿美元,但公司仍未走出亏损泥淖。
2022年至2024年截至9月30日止九个月(以下简称:报告期内),映恩生物的收入分别约为160万元(单位:人民币,下同)、17.87亿元、14.62亿元;期内亏损分别约为3.87亿元、3.58亿元、5.66亿元人民币,累计亏损13.11亿元。
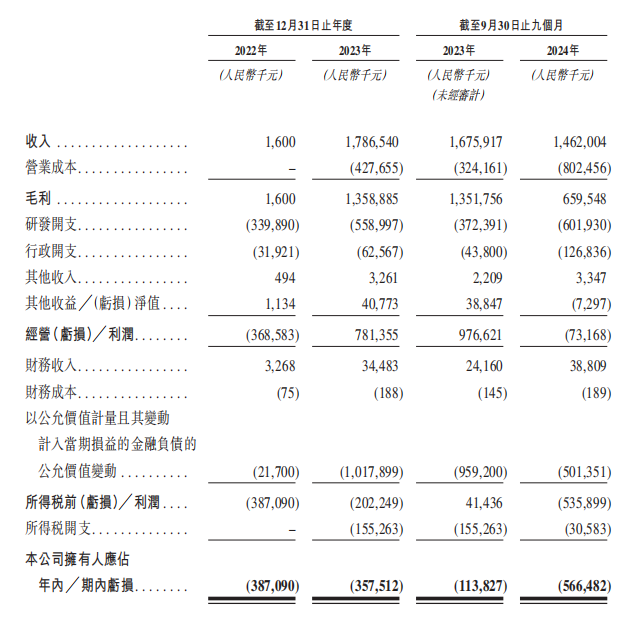
简言之,与大多数biotech一样,映恩生物同样面临资金紧张的局面。即使在实现大额授权的2023年,映恩生物仍旧亏损3.58亿元。目前映恩生物资产总值18.05亿元、负债总值则高达33.03亿元。
商业化方面,截至2月19日,公司尚未获得任何候选药物的上市批准,亦未从产品销售中获得任何收入。预计后期ADC将在未来几年实现商业化,公司计划通过选择最佳商业模式(包括建立内部商业化能力)及或与第三方(如分销商、合同销售组织及许可合作伙伴)合作)使候选药物的商业价值最大化。
根据智通财经APP观察,映恩生物持续亏损的原因,一方面在于公司需要大额研发,另一方面则是因为前期融资造成的。IPO前的各轮融资大额投资者多以优先股购入,随着估值增长,映恩生物在2023年录得大额优先股价值变动亏损10.18亿元。
尽管没有商业化产品,但是ADC出海提速为映恩生物积极“补血”。
就在今年开年,映恩生物连续完成了两笔ADC药物交易。一是将核心产品HER2 ADC药物DB-1303多个适应症在中国内地、香港和澳门的商业化权益授权给沈阳三生;另一笔交易则是将一款临床前管线DB-1418/AVZO-1418的全球范围内(大中华区除外)开发、制造和商业化权益授权给Avenzo Therapeutics,Inc.两笔交易下来,映恩生物将获得7500万美元的首付款,在未来实现开发、注册及商业化的节点还可获得里程碑付款。
Biotech授权出海浪潮席卷仍需关注商业化进程
ADC药物海外交易日趋火热。据市场不完全统计,2024年全年至少有14款ADC药物达成海外交易,其中近一半药物的交易总金额超过10亿美元。
而在Biotech授权出海浪潮下,不乏佼佼者。
比如,2023年底,百利天恒与百时美施贵宝(BMS)就BL-B01D1达成潜在84亿美元的重磅交易,打破了国产创新药出海授权纪录。
值得一提的是,百利天恒的BL-B01D1也是一款可靶向EGFR和HER3的双抗ADC药物,相比映恩生物的DB-1418研发进度更快,正在中国和美国进行超过20项针对多种肿瘤类型的临床试验,拥有的5项适应症被纳入突破性治疗品种名单。
这种情况下,映恩生物显然面临不小的竞争压力。
另外,以映恩生物的管线布局来看,其既有已经过验证的成熟靶点HER2、TROP2,也有新兴靶点B7-H3、HER3等,此后还布局了双抗ADC(如DB-1419),及针对自免疾病的ADC(如DB-2304)。
在进度和差异化开发策略上,以靶向HER2的DB-1303为例,其首个适应证为HER2表达EC,避开了与已上市药物撞车,目前正处于全球单臂2期注册研究阶段,最早将于2025年向FDA(美国食药监局)申报加速批准。就HER2 ADC全球市场容量来看,预计该市场自2023年至2028年及自2028年至2032年将分别按30.8%及16.8%的年复合增长率增长,并于2032年达到345亿美元。
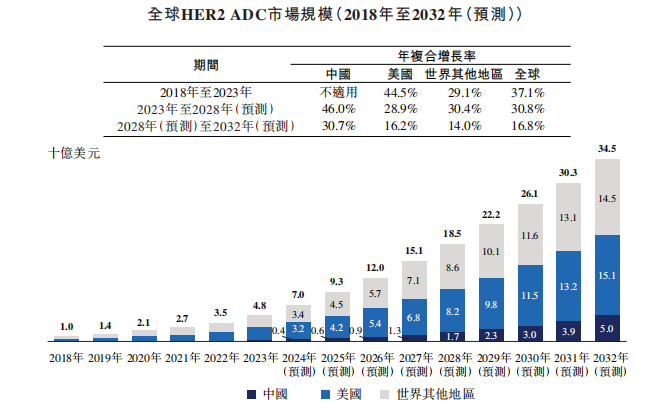
就竞争格局来看,截至最后实际可行日期,在美国有两款HER2 ADC(即Enhertu®及Kadcyla®)获批,而在中国则另有一款HER2 ADC(即爱地希®)获批。截至同日,有三款HER2 ADC(包括Enhertu®)正处于全球多区域临床试验(MRCT)阶段的III期临床开发或更后的阶段。诸多竞争对手林立,可见映恩生物的市场化进程并不算早。
综上,由于映恩生物的产品尚未商业化,研发投入加上前期融资带来的优先股价值变动,公司难掩亏损。但是ADC出海为公司带来入账,一定程度上缓解其流动性压力。其而从招股书来看,公司多数管线产品均处于临床早期,因此在竞争激烈的ADC技术平台能否脱颖而出,依然要看其后续研发实力和市场表现。