若问过去两年中国医药产业最丰硕的果实是什么?ADC药物绝对堪称“顶尖”。
从2021年荣昌生物维迪西妥单抗以26亿美元授权出海,到2022年科伦博泰与默沙东达成总金额超百亿美元的ADC合作,再到2023年百利天恒凭借双抗ADC与BMS签下单个项目84亿美元的“天价交易”,国产ADC的License out纪录一次次刷新行业认知。
巨额BD交易引发资本蜂拥而入,国产ADC赛道管线如雨后春笋般激增,行业甚至喊出“弯道超车国际巨头”的豪言。但风最会过去,当潮水逐渐退去,诸多问题逐渐浮出水面:一些被寄予厚望的ADC管线进展迟缓,部分授权项目惨遭退货,靶点同质化严重、研发瓶颈等短板尽显。
随着热度降温,资本也开始变得理性,不少ADC企业遭遇融资困难、现金流告急,部分药企更是无奈砍掉ADC管线,中国ADC行业泡沫的裂痕初现。
01
资本幻觉
2019年,是ADC发展历程中的重要分水岭。
在这一年,Polivy、Padcev、Enhertu三款ADC获批,其中第一三共与阿斯利康携手打造的 Enhertu,堪称ADC领域的“标杆药物”。它的意义非凡,不仅在临床治疗与商业推广上成绩斐然,更重要的是革新了ADC药物的开发思路。从最初针对单一靶点的“精准武器”,进阶成为基于生物标志物的“平台化治疗系统”,拉开了精准医学的“生物导弹”时代大幕。
Enhertu获批后,ADC瞬间跃升为生物创新药投资领域最炙手可热的赛道之一。海外跨国药企纷纷入局:辉瑞豪掷430亿美元收购 Seagen,吉利德以210亿美元并购 Immunomedics,艾伯维斥资101亿美元拿下 ImmunoGen,默沙东分别与科伦博泰、第一三共达成超百亿美元合作,BMS与百利天恒也达成了 84 亿美元的授权交易。
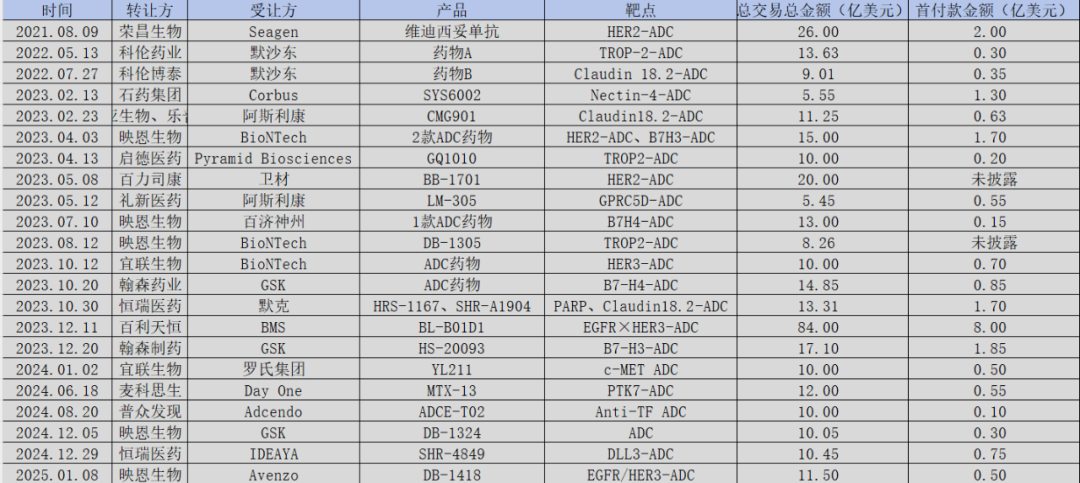
图:中国ADC管线BD一览,来源:锦缎研究院
这些国际医药巨头的大动作,被中国药企视作“技术变现”的绝佳范例。受此影响,2020年国内ADC领域融资额一举突破360亿元,荣昌生物、科伦博泰等企业通过License out协议获得数亿美元首付款,资本市场更是将ADC奉为 “确定性最高的赛道”
在这样的大环境下,市场对于ADC药物的前景预期也被无限拉高。根据Frost&Sullivan的预测,全球ADC药物市场规模在未来几年将显著扩张。2022年,全球ADC市场规模达到79亿美元,在2018—2022年间实现了40.4%的复合年增长率。展望未来,预计到2030年,全球ADC市场规模有望攀升至647亿美元,复合年增长率将达到30%。
在资本的狂热追捧与跨国药企的示范带动下,中国ADC行业呈现出一种虚假繁荣的景象。众多药企为迎合资本与跨国药企,盲目跟风布局热门靶点。部分企业自身研发实力不足,却试图通过包装项目、夸大预期来吸引投资,使得市场上充斥着大量看似前景无限,实则竞争力匮乏的项目。据统计,国产ADC新药研发达到惊人的500多项,大概占全球管线的40%。
但实际上,ADC药物的技术门槛被集体低估。ADC研发需要巧妙平衡抗体、连接子、毒素三者间的稳定性与毒性,这一过程极为复杂,研发生产技术难度大,成本非常高。以连接子技术为例,国际巨头第一三共的DXd平台经过20年迭代才实现精准可控的药物释放。部分国内企业采取“微创新”策略规避国外专利限制,或者直接外购技术,缺乏真正意义上的自主创新,这导致药物在疗效与安全性方面难以实现突破,临床失败率居高不下。
资本幻觉,为后续泡沫的破裂埋下了隐患。
02
中国ADC开始退潮
国内ADC领域表面繁荣背后,行业的根基并不稳固,资本热潮一旦退去,各类深层次问题便纷纷暴露。
今年3月20日,美国生物技术公司Elevation Oncology宣布终止Claudin18.2 ADC药物EO-3021(SYSA1801)的全球开发,并将资源转向HER3 ADC新药EO-1022。消息一出,Elevation股价单日暴跌超40%,市值蒸发近半。不仅如此,因EO-3021源于中国石药集团授权,更是引发了市场对中国创新药临床数据可信度的连锁性质疑。
EO-3021是石药集团自主研发的首款ADC药物,早在2020年 11月就获得 FDA 授予针对胃癌治疗的孤儿药资格,并于2021年先后在中国和美国获批开展临床研究。2022年7月,Elevation以 2700万美元首付款,外加最高11.48亿美元里程碑付款以及净销售额特许权使用费的条件,获取了EO-3021在大中华区以外的开发权益。
起初,EO-3021在中国启动的I期试验初步临床数据颇为亮眼,在17例可评估药效的胃癌患者中,ORR为47.1%,DCR为64.7%。然而,美国开展的临床Ⅰ期结果却不尽如人意,在36名可评估的胃癌患者中,ORR仅为 22.2%,DCR为72.2%。尽管安全性尚可,但对比其他竞品,疗效明显缺乏竞争力。
事实上,EO-3021并非首个被“终止”的中国Claudin 18.2 ADC。2024年8月,默沙东宣布退回科伦博泰SKB315(Claudin18.2)的权益;紧接着10月,BMS也将礼新医药同靶点的ADC药物LM-302权益退回。值得注意的是SKB315和LM-302并非临床早期的产品,分别已处于临床II期及III期研究阶段。
而曾经被誉为国产“ADC一哥”的荣昌生物,如今也陷入诸多困境。核心人员何如意离职,其首个国产ADC药物维迪西妥单抗,在辉瑞收购Seagen后,在2024年被辉瑞计提2亿元无形资产减值。
除此之外,诸多国内ADC项目接连受挫。百奥泰的BAT8001(HER2 ADC)在乳腺癌III期临床试验中未达到主要终点,耗费2亿多人民币后无奈终止开发;东曜药业自主研发的TAA013(HER2 ADC),因市场竞争格局改变,终止III期临床试验;宜联生物的 YL202(HER3 ADC)因安全性问题,被FDA部分暂停I期临床;信达生物从赛诺菲引进的CEACAM5 ADC,由于III期试验未达终点,也被终止开发。
在出海方面,2023年达到巅峰之后,2024年的ADC出海似乎被按下了暂停键。根据Insight数据库的统计,2024年国内ADC出海数量23个,相比2023年,交易数量持平,但重磅项目大幅缩水,总金额下降至134亿美元,较2023年下滑43%,交易首付款只有3.7亿美元,相较2023年下降了78%。
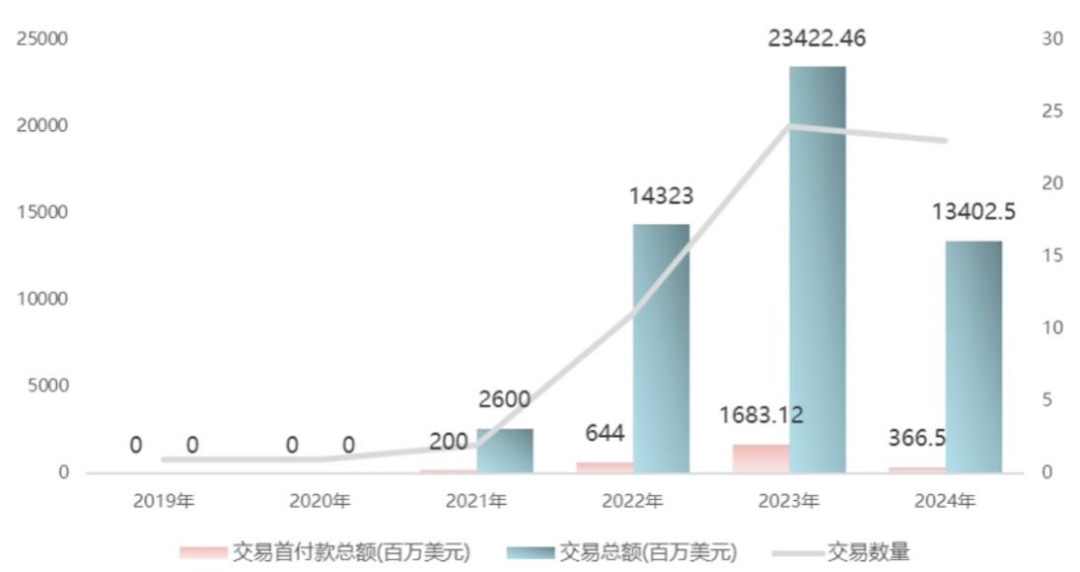
图:历年ADC出海数据汇总,来源:Insight数据库
一系列数据表明,中国ADC的表现远没有表面看上去的那么风光。
03
泡沫破裂的底层逻辑
ADC赛道骤然降温的表象之下,埋藏着更深层次的产业逻辑变革。
当跨国药企挥舞的支票簿逐渐合拢,中国创新药企才惊觉自己正站在时代转折的十字路口,资本狂欢塑造的虚假繁荣,终究敌不过医药研发的底层规律。
全球生物医药投资风向的转变率先吹响。ADC曾凭借其创新性的治疗理念与亮眼的临床数据,成为生物医药领域的热门赛道,但2024年起,全球医药投资风向已悄然转向GLP-1类药物、双抗及基因治疗领域。
诺和诺德的司美格鲁肽年销售额达到293亿美元,几乎追平药王“K药”,资本对ADC的热情被迅速分流:恒瑞医药以“NewCo”模式将三款GLP-1研发管线对外授权,获得1亿美元的首付款和后续总计60多亿美元的里程碑款;联邦制药将一款长效 GLP-1R/GIPR/GCGR 三靶点激动剂海外权益授予诺和诺德,获得2亿美元首付款以及潜在18亿美元里程碑付款,另含销售分成。
双抗领域的BD交易更加活跃。默沙东以5.88亿美元的预付款和27亿美元的里程碑付款拿下礼新医药的LM-299;BioNTech以9.5亿美元收购成立仅6年的普米斯;宜明昂科以21.5亿美元的总金额将IMM2510授权给Instil Bio。此外,同润生物、嘉和生物、岸迈生物、康诺亚、百奥赛图等企业,也纷纷通过license out双抗产品,收获了数亿美元的收益。
如果说风口转移只是行业发展的正常周期波动,那么同质化竞争引发的内卷旋涡则加速了泡沫破裂。有别于全球市场,国内ADC在强确定性靶点的研发竞争上更为激烈,超过50%的ADC管线集中于 HER2、TROP2、Claudin18.2 等前五大靶点。以HER2、TROP2、CLDN18.2这三个靶点为例,国内ADC候选药物数量在全球管线数量中的占比,分别高达63.6%、76.5% 和85.7%。
这种同质化的竞争导致患者招募困难,临床试验周期延长,研发成本大幅增加。不同企业的ADC产品在临床试验中相互竞争患者资源,使得入组难度加大,许多试验不得不降低入组标准或延长招募时间,这不仅耗费更多资金,还可能影响试验结果的准确性与可靠性。
另一方面,大量同质化产品的出现,使得市场对单个产品的价值评估降低。当众多企业的产品都针对同一靶点,且疗效与安全性并无显著差异时,即便有产品成功上市,也将面临激烈的市场竞争,难以获得理想的市场份额与商业回报。
与此同时,跨国药企大多已构建起成熟靶点的ADC管线,在靶点选择上变得愈发挑剔。例如,默沙东以40亿美元的预付款,总计220亿美元总金额从第一三共引进的三款ADC,分别靶向HER3、B7-H3和CDH6,属于新兴或冷门靶点,且临床进度均已推进至全球前三。对于那些同质化竞争激烈、临床进度滞后的靶点,跨国药企宁可放弃首付款,也会果断选择放弃。
作为甲方的MNC,终究掌控着核心话语权。
04
追风出不来巨头
中国ADC的泡沫破裂,既是一场资本的退潮,更是一次行业价值体系的重构。
回顾近几年中国ADC行业的License out模式,长期遵循“高总金额、低首付”的叙事逻辑,这种设计表面看似为国内药企描绘了巨额收益的蓝图,实则暗藏风险分配的高度不对等。以石药集团Claudin 18.2 ADC为例,其与Elevation的合作首付款仅2700万美元,占总交易额2.3%,后续的11.68亿美元里程碑付款需要跨越三期临床试验到商业化阶段才能获得,这意味着当项目推进受阻时,Elevation可随时以“战略调整”为由终止合作,并只需要付出极小的代价。
这种模式正在严重扭曲中国ADC创新的价值。当MNC通过小额首付款批量“扫货”中国ADC管线时,实质上是在进行创新资产的“风险对冲式采购”,用微小的首付成本来锁定潜在的优质资产。而中国创新药企却陷入“卖青苗”的困境,难以凭借创新成果收获与之匹配的回报。并且一旦管线失败,企业不仅失去现金流,更面临市场信心的崩盘。
恒瑞医药的“NewCo”模式则给了中国ADC出海新的启发,通过与MNC共同设立新的海外公司,以股权绑定实现从单纯技术授权向战略共生转变,联合组建全球研发团队,共享数据资源,最大化挖掘创新价值。
另一方面,中国创新药企要清楚认识到,License-out虽可解一时之困,是穿越寒冬的“救命稻草”,但自主商业化才是立足全球市场的终极答案。中国ADC若想在国际竞争中比肩第一三共等巨头,不仅要加大研发投入,还需构建海内外营销网络,如百济神州自主推广泽布替尼,持续提升产品国际认可度,实现从“卖技术”到“创品牌”的跨越。
这就更要求创新回归本真,药企必须跳出“跟随式创新”陷阱,自主搭建核心技术平台,进行差异化探索,精准对接未满足的临床需求。比如,宜联生物自主开发的三肽连接子TMALIN,具有独特的酶切特性,具有在肿瘤微环境中胞外裂解的能力,无论抗体是否可被内吞,ADC都仍具有较高的抗肿瘤活性,大大拓宽了抗体的选择范围。基于TMALIN技术平台,宜联生物开发十多款进入临床阶段的ADC药物,其中不乏NaPi2b、DLL3、MSLN、LRRC15等差异化靶点。
中国ADC行业泡沫的破裂并非终点,而是价值重构的起点。当风口退去,唯有真正具备平台创新、临床洞察和全球商业能力的药企才能穿越周期。